Λίγοι άνθρωποι συνειδητοποιούν ότι η Άδεια Χρήσης Έκτακτης Ανάγκης (EUA) του εμβολίου Pfizer/BioNTech Covid-19/BNT 162b2 χορηγήθηκε με βάση τα δεδομένα αποτελεσματικότητας 170 ασθενών. Οι 162 που έλαβαν το εικονικό φάρμακο και οι 8 ασθενείς που εμβολιάστηκαν αποτέλεσαν τη βάση των ισχυρισμών της 95% αποτελεσματικότητας του εμβολίου.
- Από την Jeyanthi Kunadhasan («Spectator Australia»)
Δεν έχει γίνει πολλή συζήτηση για αυτούς τους ασθενείς. Από πού προέρχονται; Θα μπορούσαμε να είχαμε ένα κατά προσέγγιση χρονοδιάγραμμα ως προς το πότε θα έπρεπε να είχαν συγκεντρωθεί όλοι αυτοί οι ασθενείς;
Το τελικό στάδιο της δοκιμής Pfizer/BioNTech ήταν η μόλυνση από Covid-19 τουλάχιστον επτά ημέρες μετά τη δεύτερη δόση και η αποτελεσματικότητα του εμβολίου μετρήθηκε υπολογίζοντας τον κίνδυνο ασθένειας μεταξύ εμβολιασμένων και μη εμβολιασμένων ατόμων και προσδιορίζοντας το ποσοστό μείωσης του κινδύνου ασθένειας μεταξύ εμβολιασμένων ατόμων σε σχέση με τα μη εμβολιασμένα άτομα.
Οι 170 ασθενείς βρέθηκαν, θαμμένοι βαθιά ανάμεσα στις εκατοντάδες χιλιάδες σελίδες και η ύπαρξη των οποίων διατέθηκε μόνο κατόπιν δικαστικής απόφασης.
Σε μία ανάλυση που δημοσιεύτηκε στο dailyclout.io, οι συνεργάτες μου και εγώ εξετάσαμε τις λεπτομέρειες του τρόπου με τον οποίο βρέθηκαν αυτοί οι ασθενείς. Επίσης, διασταυρώσαμε τη λίστα μας με δημογραφικά δεδομένα που είναι διαθέσιμα στο κοινό, τα οποία ταίριαξαν απόλυτα. Ως εκ τούτου, είμαστε βέβαιοι ότι η λίστα μας με τους 170 ασθενείς, που είναι δημόσια διαθέσιμη στο άρθρο μας σε μορφή εγγράφου excel, είναι στην πραγματικότητα οι 170 που αποτέλεσαν τη βάση των ισχυρισμών περί «αποτελεσματικότητας» και «ασφάλειας» του εμβολίου.
Σύμφωνα με το επιστημονικό πρωτόκολλο της δοκιμής, μια σημαντική απόκλιση πρωτοκόλλου αποτελεσματικότητας στον αξιολογήσιμο πληθυσμό θα απέκλειε έναν συμμετέχοντα από την τελική ανάλυση μετά τη δοκιμή. Αυτό είναι λογικό, εάν πρόκειται να δηλώσε κάποιος ότι ένα φάρμακο είναι αποτελεσματικό. Θα ήθελε να το κάνει με βάση έναν πληθυσμό που θα είχε περάσει σωστά το πρωτόκολλο δοκιμής και δεν θα πληρούσε κανένα από τα κριτήρια αποκλεισμού που θα είχαν οριστεί εκ των προτέρων στο πρωτόκολλό.
Ευρήματα
Τι βρήκαμε στους 170 ασθενείς; Ένας από τους 170 δεν έλαβε τη σωστή δόση του υπό έρευνα προϊόντος, ένας άλλος έλαβε ένα προϊόν αίματος εντός 60 ημερών που αποτελεί σημαντική απόκλιση από το πρωτόκολλο. Άλλοι δύο αποσύρθηκαν από τη δοκιμή πριν από την ημερομηνία έκδοσης της EUA (Εξουσιοδότηση χρήσης έκτακτης ανάγκης), αλλά εξακολουθούσαν να περιλαμβάνονται στους 170 (ένας από αυτούς διαφώνησε με τον τρόπο με τον οποίο αντιμετωπίστηκε ιατρικά στη δοκιμή).
Σημειώσαμε επίσης πώς το μεσοδιάστημα δοσολογίας (που δηλώθηκε στο πρωτόκολλο ότι ήταν 21 ημέρες, με επιτρεπόμενο όριο 19-23 ημερών μεταξύ της δόσης 1 και 2) διευρύνθηκε περιέργως σε 19-42 ημέρες.
Δείχνουμε στην εργασία μας, πώς τουλάχιστον 1.410 ασθενείς που διαφορετικά θα θεωρούνταν ως «αποκλίσεις πρωτοκόλλου» λόγω αποτυχίας χορήγησης του φαρμάκου εντός του μεσοδιαστήματος δοσολογίας των 19 έως 23 ημερών θα μπορούσαν να συμπεριληφθούν σε μια τελική ανάλυση εάν διευρυνόταν σε 19-42 ημέρες. Το πιο σημαντικό, αυτό περιελάμβανε 5 από τους 170 ασθενείς.
Το σχέδιο στατιστικής ανάλυσης επιτρέπει τροποποιήσεις στο πρωτόκολλο, όπου αυτό κρίνεται σκόπιμο. Αλλά δηλώνει παράλληλα ότι σημαντικές τροποποιήσεις θα πρέπει να αντικατοπτρίζονται εμφανέστατα σε μια τροποποίηση πρωτοκόλλου. Ποτέ δεν υπήρξε επίσημη τροποποίηση πρωτοκόλλου, και στις 14 εκδόσεις του, που να επισημοποιεί ένα διάστημα δοσολογίας 19-42 ημερών. Στην πραγματικότητα, η τροποποίηση του πρωτοκόλλου 5, (στις 24 Ιουλίου 2020), που έγινε 3 ημέρες πριν από την επίσημη έναρξη των τμημάτων της φάσης 2/3 της δοκιμής, αναφέρει ρητά το διάστημα 21 ημερών μεταξύ των 2 δόσεων.
🚨🚨🚨
Unbelievable.
Dr. Renata Moon, board certified pediatrician, found an intentionally blank package insert in a box of mRNA vaccine product she planned to administer to a child.
This is what passes as “informed consent” under the leadership of the COVID cartel. pic.twitter.com/JVuY2QU00T
— Senator Ron Johnson (@SenRonJohnson) December 7, 2022
Ερωτήματα
Τίθεται το ερώτημα γιατί ήταν σκόπιμο να διευρυνθεί το διάστημα δοσολογίας ενός νέου φαρμάκου και πως τα κλινικά δεδομένα υποστηρίζουν αυτή την κίνηση; Δεν θεωρείται σημαντική τροποποίηση η διεύρυνση του διαστήματος δοσολογίας ενός νέου φαρμάκου στην πρώτη δοκιμή αυτού του φαρμάκου;
Οι προηγούμενες φάσεις αυτής της δοκιμής χρησιμοποιούσαν επίσης ένα μεσοδιάστημα δοσολογίας 21 ημερών. Επιτρεπόταν σκόπιμη ασάφεια στο πρωτόκολλο με τον μη καθορισμό αριθμού στις λέξεις «προκαθορισμένο παράθυρο ημερομηνιών» για το διάστημα δοσολογίας. Το παράθυρο 19–42 ημερών εμφανίστηκε μόνο στην τεκμηρίωση ως προς την Εξουσιοδότηση χρήσης έκτακτης ανάγκης. Το γεγονός αυτό θέτει υπό αμφισβήτηση την έννοια της λέξης «προ». Πότε ορίζετε ένα «προκαθορισμένο παράθυρο ημερομηνιών» εάν είναι φαινομενικά καθορισμένο μετά τη δοκιμή; Και πάλι, αυτό εξηγείται με μεγάλη λεπτομέρεια στο άρθρο μας.
Από πού προήλθαν αυτοί οι ασθενείς; Ένας άλλος ερευνητής δεδομένων ευγενικά χαρτογράφησε τους 170 ασθενείς στις διάφορες τοποθεσίες της έρευνας. Θα περίμενε κανείς μεγαλύτερη συνεισφορά από τις πιο πυκνοκατοικημένες περιοχές των Ηνωμένων Πολιτειών ως προς τους 170 ασθενείς, καθώς πρόκειται για μια εξαιρετικά μεταδοτική ασθένεια. Ωστόσο, η Αργεντινή συνεισέφερε σε 36 από τις 170 περιπτώσεις.
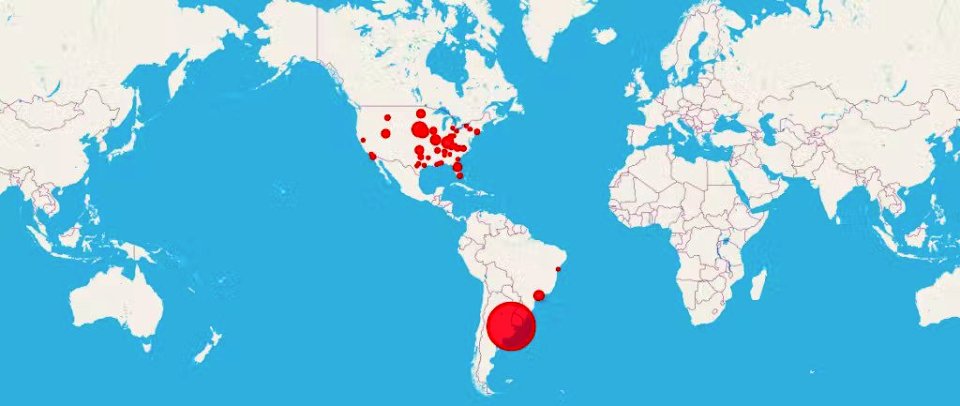
Βρήκαμε επίσης 6 ζεύγη διαδοχικών αριθμών στη λίστα μας. Σε μια πραγματικά τυχαιοποιημένη ελεγχόμενη δοκιμή, κάθε ασθενής θα πρέπει να έχει ίσες ευκαιρίες να επιτύχει ως προς το τελικό στάδιο της δοκιμής. Καλούμε τους μαθηματικούς να υπολογίσουν την πιθανότητα 6 ζευγών διαδοχικών αριθμών να εμφανίζονται σε μια λίστα 170 από έναν δυνητικό πληθυσμό περίπου 37.000 (τελικός πληθυσμός κατάλληλος για ανάλυση) σε ένα πραγματικό τυχαίο δείγμα.
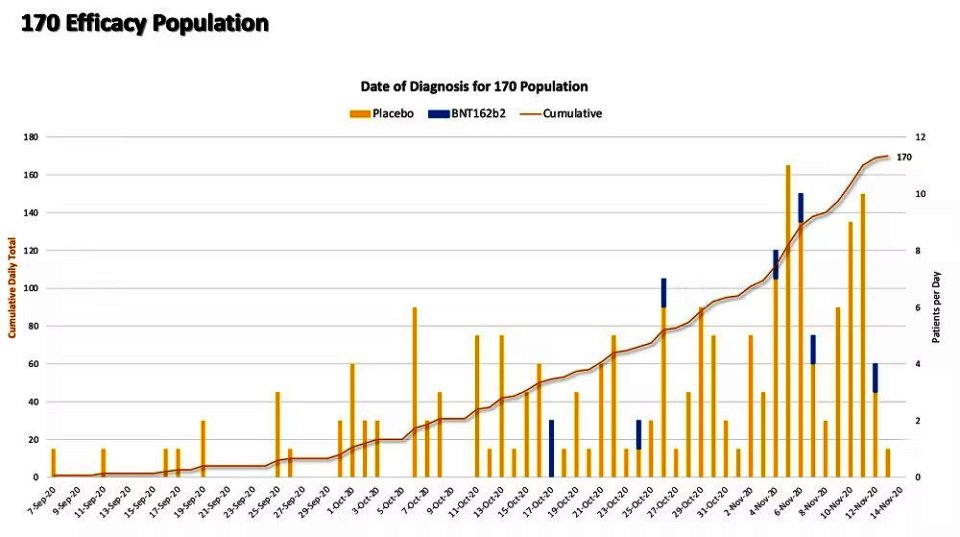
Από τη δημοσίευση της αρχικής εργασίας, έχουμε έκτοτε αναλύσει το ποσοστό συγκέντρωσης του πληθυσμού των 170 σε σχέση με την ημερομηνία λήξης δεδομένων της 14ης Νοεμβρίου 2020. Αυτή είναι μια κατά προσέγγιση ανάλυση, καθώς η ημερομηνία διάγνωσης δεν τεκμηριώθηκε ομοιόμορφα. Σε κάποιες περιπτώσεις, πήραμε σαν βάση την ημερομηνία λήψης δείγματος με μπατονέτα ως αντιπροσωπευτικό της ημερομηνίας διάγνωσης.
Ανάλυση
Για να κατανοήσουμε το ζήτημα στα πλαίσια του, πρέπει να εξοικειωθούμε με το σχέδιο ανάλυσης που η Pfizer καθόρισε στο πρωτόκολλο της, δίνοντας ιδιαίτερη προσοχή στα όρια για την ενδιάμεση ανάλυση, καθώς και στα όρια αποτελεσματικότητας και αναποτελεσματικότητας που ορίζονται. Για παράδειγμα, εάν 54 εμβολιασμένα άτομα είχαν διαγνωστεί με Covid από 164 ασθενείς στον αξιολογήσιμο πληθυσμό, αυτό το φάρμακο δεν θα είχε δηλωθεί αποτελεσματικό στην πρόληψη κατά της μόλυνσης.
Με την ανάλυσή μας ως προς τα δεδομένα της Pfizer, γεννιώνται ερωτήματα για το πότε έγινε η ενδιάμεση ανάλυση. Γιατί το φάρμακο δεν δηλώθηκε αποτελεσματικό όταν 62 περισσότερες περιπτώσεις, κατάλληλες για το τελικό σημείο της δοκιμής, θα είχαν συσσωρευτεί ως την τελευταία περίπου εβδομάδα του Οκτωβρίου 2020; Το όριο για τη μη αποτελεσματικότητα του φαρμάκου σε αυτό το στάδιο ήταν να εμβολιαστούν περισσότεροι από 15 στον επιλέξιμο πληθυσμό τελικού σταδίου.
Στην τεκμηρίωση της EUA (Εξουσιοδότηση χρήσης έκτακτης ανάγκης), αναφέρθηκε ότι η ημερομηνία αποκοπής των δεδομένων για την πρώτη ενδιάμεση ανάλυση ως προς την αποτελεσματικότητα ήταν η 4η Νοεμβρίου 2020, όταν θα είχαν συγκεντρωθεί συνολικά 94 επιβεβαιωμένα κρούσματα COVID-19. Υπολογίσαμε ότι περίπου 112 περιπτώσεις θα έπρεπε τελικά να είχαν συγκεντρωθεί έως τις 4 Νοεμβρίου 2020. Οι ερευνητές είπαν δημόσια ότι δεν ήταν σε θέση να κάνουν την πρώτη ενδιάμεση ανάλυση που είχε προγραμματιστεί με τη συγκέντρωση 32 επιλέξιμων υποθέσεων. Δημόσια, επίσης, η πρώτη ενδιάμεση ανάλυση έγινε στις 4 Νοεμβρίου 2020. Δεν είχε γίνει ενδιάμεση ανάλυση πριν από αυτή; Γιατί;
Υπήρξε κάποιο ζήτημα σε αυτούς που δεν μπήκαν στους 170; Η ομάδα δεδομένων στο DailyClout.io ανάλυσε τους αποκλεισμένους ασθενείς της δοκιμής.
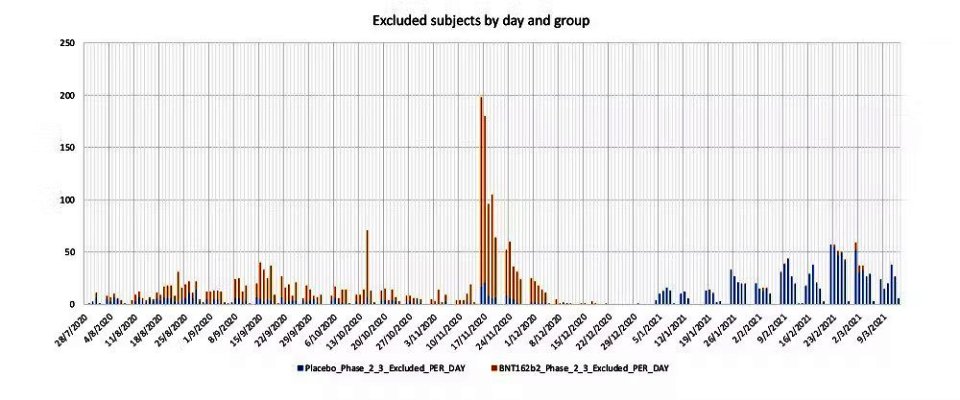
Συνδυάζοντας τα δύο, μαζί με ορισμένα σημαντικά στοιχεία στο χρονοδιάγραμμα, μπορούμε να δούμε πριν από την έκδοση της EUA (Εξουσιοδότηση χρήσης έκτακτης ανάγκης) δυσανάλογα περισσότερους εμβολιασμένους ασθενείς να έχουν αποκλειστεί από τη δοκιμή. Τουλάχιστον, θα πρέπει να υπάρξει πρόσβαση στα αρχεία των συγκεκριμένων αποκλεισμένων ασθενών.
Η μεγαλύτερη απότομη αύξηση που βλέπουμε στο γράφημα δείχνει ότι 181 (0,9%) ασθενείς αποκλείστηκαν από την ομάδα εμβολίων τη Δευτέρα 16 Νοεμβρίου 2020, αμέσως μετά την ημερομηνία λήξης δεδομένων της 14ης Νοεμβρίου 2020. Στο παρακάτω γράφημα, επίσης διακρίνονται οι εξαιρέσεις της δοκιμής έναντι του χρονοδιαγράμματος προσαύξησης του πληθυσμού των 170.
Ανωμαλίες
Ήταν ενήμερη η αυστραλιανή TGA (αντίστοιχη του αμερικάνικου FDA) για τις ανωμαλίες που εντοπίστηκαν στους 170 ασθενείς που αποτέλεσαν τη βάση του ισχυρισμού αποτελεσματικότητας του εμβολίου ώστε να δοθεί εξουσιοδότηση χρήσης έκτακτης ανάγκης; Ως αναισθησιολόγος που απολύθηκε εξαιτίας της υποχρεωτικότητας των εμβολιασμών κατά της Covid-19, αποτελεί ακόμα μια μεγαλύτερη φάρσα για εμένα ότι στους ασθενείς που θα λάμβαναν τους υπηρεσίες μου δεν δόθηκε ούτε καν η σωστή δόση του υπό έρευνα φαρμάκου.
Με την ανάλυσή μας, τουλάχιστον 7 έως 9 ασθενείς δεν θα έρπεπε να αποτελούν μέρος της τελικής ανάλυσης αποτελεσματικότητας στην οποία βασίστηκε η έγκριση αυτού του φαρμάκου. Αυτός ο αριθμός θα οδηγούσε έριχνε το όριο κάτω από τις 164 επιλέξιμες υποθέσεις.
Η βάση βάσει της οποίας εκδόθηκε η EUA πρέπει να επανεξεταστεί. Τόσα πολλά επιστημονικά πρότυπα έχουν καταρριφθεί σε αυτήν την πανδημία, η διεξαγωγή κλινικών δοκιμών είναι ένα από αυτά…
*αναδημοσίευση από το kourdistoportocali.com

